Термодинамика.
Внутренняя энергия – это суммарная энергия хаотического движения и взаимодействия микрочастиц системы (молекул). ![]()
![]() – для идеального или одноатомного газа.
– для идеального или одноатомного газа.
![]() – для двухатомного газа.
– для двухатомного газа.
∆ U - изменение внутренней энергии тела, сопровождается изменением температуры или агрегатного состояния тела.
![]()
∆ U - два способа изменения
Для газа
А - работа газа или над газом 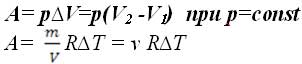
Работа газа (расширение) U↓,T↓ на графике переход 1→а→2
Работа над газом (сжатие)U↑,T↑на графике переход 2→б→1
Геометрический способ нахождения работы 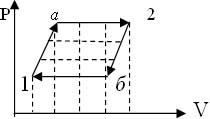
А = S площади фигуры между графиком и осью V (процесс не замкнут)
Для циклического процесса
1→а→2→б→1
Для любого тела
Q – теплопередача
1. Теплопроводность (от молекулы к молекуле)
2. Конвекция (потоками вещества)
3. Излучение (инфракрасные лучи)
1. Q = cmΔT – нагрев, охлаждение, где с – удельная теплоемкость тела [Дж/(кгС)]
2. Q = λm – плавление, кристаллизация, где λ - удельная теплота плавления (Дж/K)
3. Q = Lm–парообразование , конденсация, где L - удельная теплота парообразования (Дж/K)
4. Q = qm – сгорание топлива, где q – удельная теплота сгорания топлива (Дж/K)
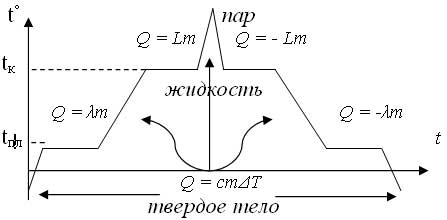
Уравнение теплового баланса для замкнутой системы тел: ± Q1 ± Q2± … ± Qn = 0
для газа
∆U = Aвнешн.с. ± Q или ∆ U = -Aгаза. ± Q
Первый закон термодинамики - изменение внутренней энергии системы происходит за счет совершения работы (газом или над газом) и теплопередачи.
Q = ∆U +A
Пример: 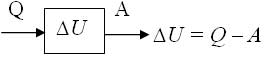
Второй закон термодинамики - невозможен процесс, единственным результатом которого была бы передача энергии от холодного тела к горячему (сформулировал этот закон Р. Клаузиус).
Зарегистрированные пользователи, предварительно войдя на сайт под своим именем, могут скачать с этой страницы полный вариант методических материалов для занятий с учащимися, состоящих из двух блоков – изложение теории и набор тестов с ответами по теме Термодинамика (ссылка на файл будет указана ниже).
- Версия для печати
- 5822 просмотра

